RNA interference
为了研究某个基因的功能,科学家经常需要降低该基因表达或者完全敲除该基因。
这两种方式针对的遗传信息处理路径不同。根据遗传信息的中心法则(图1),基因完全敲除需要敲除基因组DNA上该基因的部分或者全部信息,以阻止该基因的正常转录,进而不能表达出正确的蛋白;基因的敲低,一般是作用于mRNA上,阻遏蛋白翻译或者降解mRNA,最终导致蛋白表达水平下调。
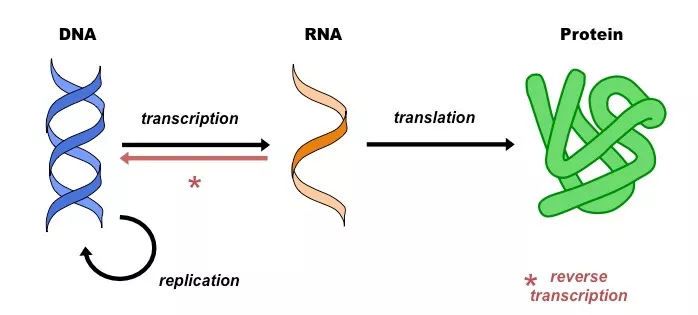
图1 遗传信息-中心法则
1、RNAi
通过降解具有同源序列靶基因的mRNA,达到阻止基因表达的作用。目前应用最为广泛的是小干扰siRNA、shRNA以及通过模拟miRNA表达产生siRNA以敲低目的基因的表达水平。
小干扰RNA(small interfering RNA,siRNA)一般是20-25bp的双链短RNA链,它一般是通过化学直接合成或者通过其它dsRNA在细胞内由Dicer酶剪切而成。在细胞内,siRNA可以与RISC复合体结合, 解开其双链,使双链RNA变为单链RNA。打开的单链RNA能够和mRNA上的互补序列结合,然后RISC复合体会切断与其互补的mRNA序列。完成这一系列操作后,RISC-siRNA复合体带着单链的siRNA,会从切断的mRNA上解脱,再去结合、继续降解靶基因mRNA(图2)。
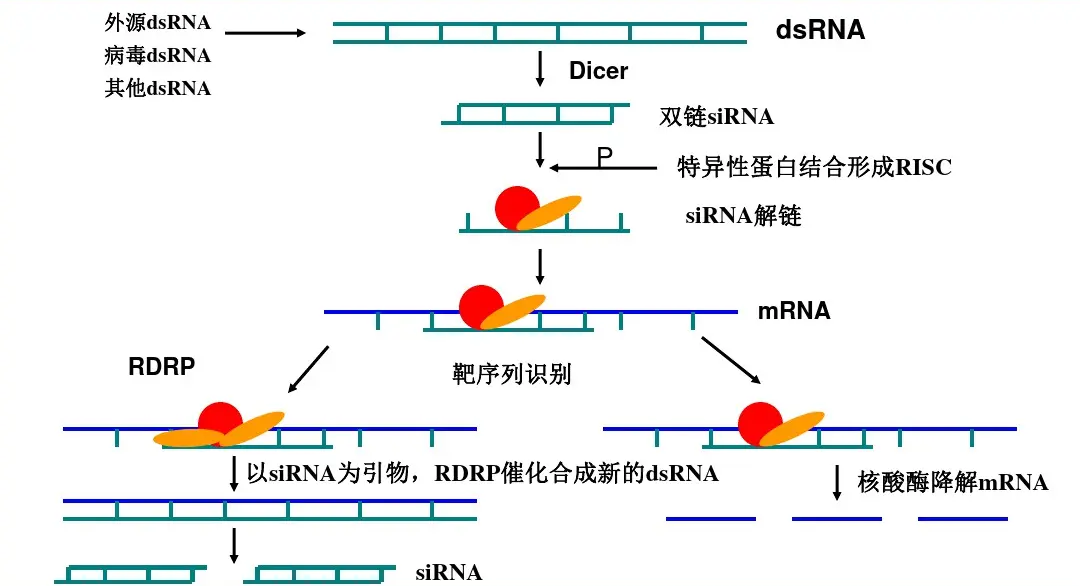
图2 RNAi作用机制
shRNA是一类很常用的siRNA的前体,通过U6或者H1转录,进而由Dicer酶剪切形成siRNA,实现对靶基因表达水平的敲低(图3)。shRNA是质粒形式,可以大量制备,并带有各种荧光或者筛选标记,亦可以包装病毒来感染细胞,增强表达能力。

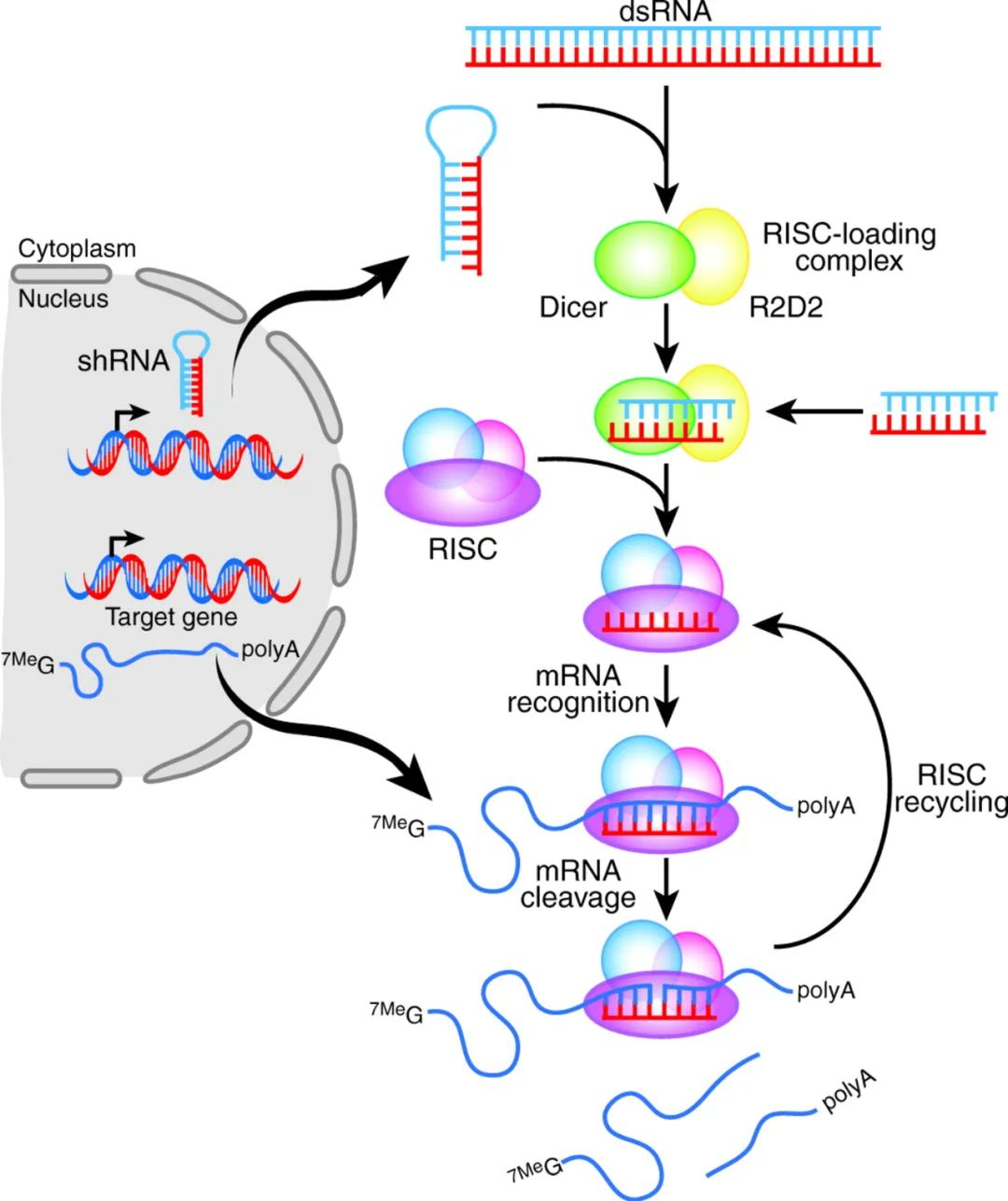
图3 shRNA结构范例及作用机制
利用miRNA产生原理,同样可以实现siRNA的敲低,而且由于miRNA是由RNA聚合酶II(polII)启动转录的,所以可以使用特异性启动子,实现细胞的特异性敲降。在细胞核内,基因组DNA 转录生成较长的RNA分子(可长达1000nt),被双链RNA 特异的核糖核酸酶 Drosha 切割成长度大约70-100 碱基的、具发夹结构的RNA 分子(前体 microRNA)。这些发夹结构的RNA 通过核输出蛋白exportin5 机制转运到细胞质,然后被第二个双链 RNA 特异的核糖核酸酶Dicer 切割,得到19-23nt 大小的成熟的microRNAss 产物。成熟的单链microRNAss 与类似RNA 诱导沉默复合物(RISC)结合,并参与 RNA 干扰反应(RNAi)(图4)。
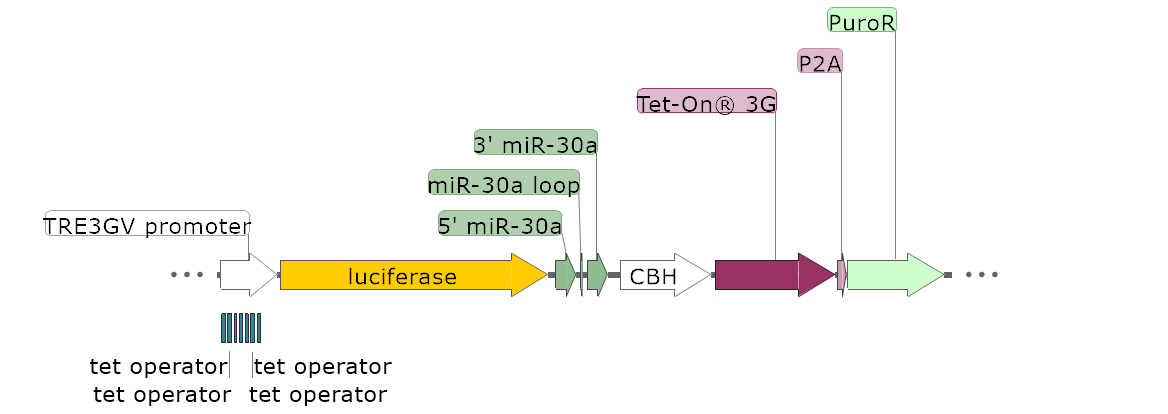
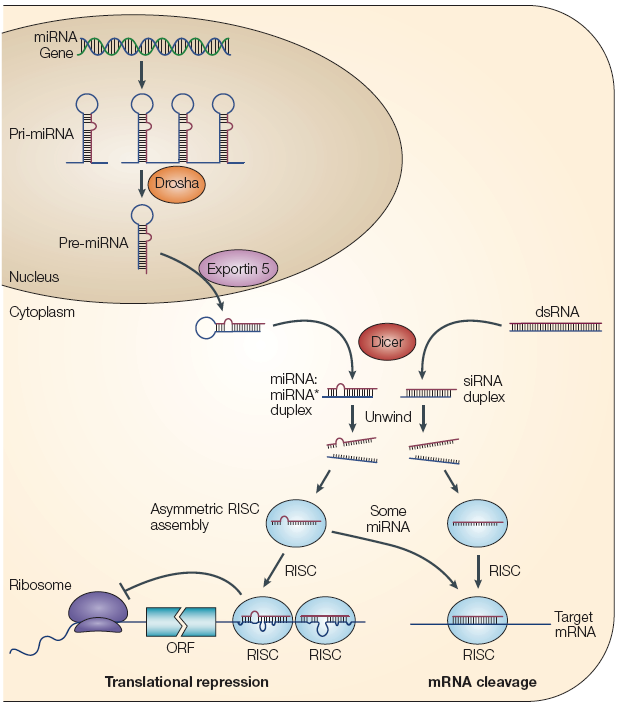
图4 mir-30a结构范例及作用机制
2、Cas9-sgRNA
CRISPR-Cas9基因编辑技术是最近几年非常火热的基因敲除技术,通过人工设计的 sgRNA(guide RNA)来识别目的基因组序列,并引导 Cas9 蛋白酶进行有效切割 DNA 双链,形成双链断裂,损伤后修复会造成基因敲除或敲入等,最终达到对基因组DNA 进行修饰的目的。该技术由于对基因组DNA进行编辑,可以使靶基因完全不能表达(图5)。
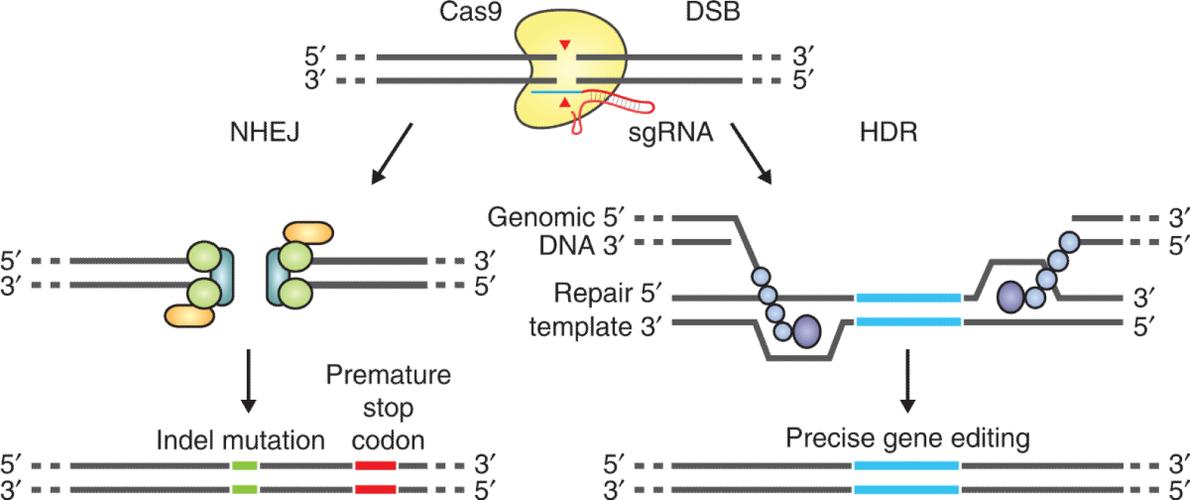
图5 Cas9-sgRNA作用机制
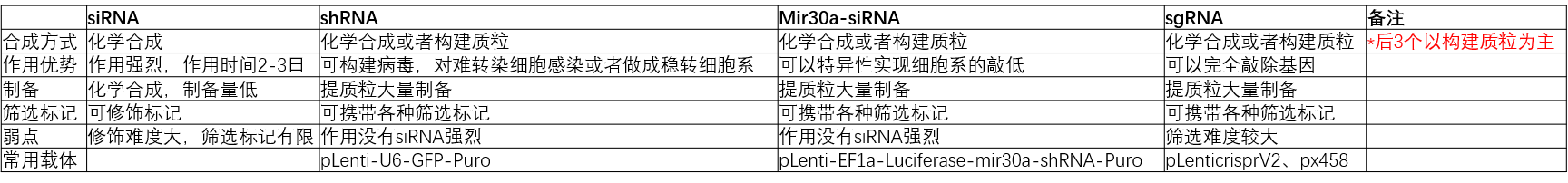
几种敲低方法优势对比